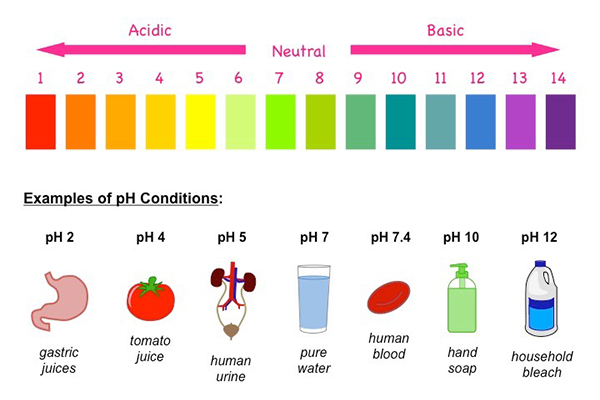
pH چیست؟
پیاچ یا پ هاش (به انگلیسی: PH) یک کمیت مهم لگاریتمی است که میزان اسیدی یا بازی بودن مواد را مشخص میکند. بیشتر آبزیان فقط در پیاچ بین ۵ تا ۹ زنده میمانند.
تعریف کوتاه و البته خلاصهٔ کاغذ پی اچ (P H): این معرف علاوه بر نشان دادن محیط اسیدی یا خنثی یا بازی میزان بازی یا اسیدی شدن محیط را هم نشان میدهد. برای مثال: رنگ کاغذ پی اچ آغشته به پرتقال نارنجی کمرنگ و آغشته به جوهر نمک قرمز پررنگ است.
مهم:اسید قوی آغشته به کاغذ پی اچ (قرمز) پررنگ و باز قوی آغشته به کاغذ پی اچ آبی پررنگ میشود.
نقش PH در سلامتی انسان، بهطور خلاصه : پایین بودن آن در بدن میتواند به مفهوم اسیدی بودن محیط اندامهای انسانی باشد و باعث پوکی استخوان شود . در صورت پایین بودن پی اچ در بدن اولین نشانههای آن پوسیده شدن دندانها بواسطه کمبود کلسیم میباشد زیرا متابولیسم بدن انسان بهطور پیوسته نیاز به محیطی خنثی یا قلیایی دارد و برای جبران آن، از استخوانها یا دندانها که منبعی سرشار از کلسیم هستند استفاده میکند و به این صورت باعث پوسیدگی استخوانها و دندانها میشود. پایین بودن پی اچ بیشتر در مادران شیرده و دختران بین سنین ۱۵ تا ۲۴ سال روی میدهد و سپس در سنین بالاتر و مخصوصاً پس از زایمان دچار بیماری پوکی استخوان میشوند. از این روی قرار داشتن PH در بدن انسان در محدوده خنثی بسیار حیاتی و مهم است.
PH:potential of hydrogen (به معنی پتانسیل هیدروژن) بررسی غلظت یون هیدروژن در آب میباشد که در اواخر سده نوزدهم برای برخی از صاحبان صنایع شیمیایی اهمیت ویژهای پیدا کرد. به عنوان مثال غلظت یون هیدروژن در طول فرایند تخمیر و فعالیت مخمرها اثر میگذارد و لازم است که غلظت یون هیدروژن دایماً مورد بررسی قرار گیرد. از طرفی چون غلظت یون هیدروژن معمولاً عددی بسیار کوچک است و کار کردن با آن دشوار است، نخستین بار سورِن سِن دانشمند دانمارکی در سال ۱۹۰۹ میلادی مقیاسی به نام pH را بنا کرد. بنا به تعریف، pH برابر منفی لگاریتم مبنای ۱۰ غلظت مولی یون هیدروژن فعال در محلول است.
در دمای اتاق(pH (298Kآب خالص را ۷ در نظر میگیریم. زیرا در این دما غلظت یون هیدرونیم در آب خالص برابر۷-۱۰است.
در دمای اتاق(۲۹۸k) گسترهٔ بازهٔ pH از (۱۴ ~ ۰) است. عدد صفر اسیدیترین محیط و عدد ۱۴ بازیترین محیط را مشخص میکند. در چنین دمایی، محلولی با pH = ۷ خنثی در نظر گرفته میشود.
با بالا بردن دما، گسترهٔ بازهٔ pH کمتر میشود. برای مثال در دمای ۳۵۸K این بازه به (۱۳~۰) تغییر میکند. در نتیجه در چنین دمایی، محلولی با pH=۶٫۵ را خنثی فرض خواهیم کرد.